3. Therapie
3.1 Behandlungsziele
Therapieziele sind neben der Verbesserung prognostisch relevanter Outcomes wie der Verhinderung von kardiovaskulären und renalen Ereignissen vor allem Symptomfreiheit, der Erhalt oder die Wiederherstellung der Lebensqualität und Vermeidung bzw. Verringerung von Sekundär- bzw. Langzeitkomplikationen. Um diese Ziele zu erreichen, ist es von Bedeutung, auch andere prognostisch relevante Begleiterkrankungen adäquat zu behandeln (z. B. Hypertonie, kardiovaskuläre Erkrankungen).
Nach den Daten vorliegender Studien werden Therapieziele immer noch in erster Linie durch eine möglichst optimale Blutzuckereinstellung erreicht. Es ist festzustellen, dass eine immer striktere Zielvorgabe des HbA1c (zum Teil < 6,5%) gefordert wird. Es konnte in der ADVANCE-Studie jedoch keine Veränderung der kardiovaskulären Endpunkte und der Mortalität für diesen angestrebten HbA1c-Wert festgestellt werden. Die 2023 aktualisierte NVL zur Therapie des Typ-2-Diabetes trägt dem mit einem individualisierten HbA1c-Zielkorridor von 6,5–8,5% Rechnung. Berücksichtigung dabei finden Lebenserwartung, Komorbidität, Polymedikation, Hypoglykämierisiko etc. [5].
3.2 Nichtmedikamentöse Therapie
Die nicht-medikamentöse Basistherapie mit dem Ziel einer Lebensstiländerung bietet eine wirkungsvolle Therapieoption (z.B. Steigerung der körperlichen Aktivität, Ernährungsumstellung, Reduktion von Übergewicht). Sie ist Grundlage einer jeden Behandlung. Erst wenn nicht-medikamentöse Maßnahmen ausgeschöpft sind, sieht die NVL-Leitliniengruppe die Indikation zur medikamentösen Therapie. Auch die Fachinformation der verschiedenen zugelassenen Medikamente zur Behandlung von Diabetes sieht die jeweilige Verordnung erst dann als indiziert an, wenn Bewegung und Diät keinen ausreichenden Erfolg gebracht haben. Zudem sollen Diät und Bewegung immer als ergänzende Maßnahme angewandt werden.
3.3 Medikamentöse Therapie
Die medikamentöse Therapie des Diabetes mellitus hat in den letzten zehn Jahren insgesamt weiter zugenommen. Die Antidiabetika haben mit 3,6 Mrd € im Jahr 2023 den zweithöchsten Nettokostenzuwachs (+18,1%) gegenüber dem Vorjahr und damit Rang 3 der umsatzstärksten Arzneimittelgruppen erreicht. Innerhalb der antidiabetischen Wirkstoffgruppen lassen sich deutliche Verordnungstendenzen feststellen. So zählen zu den rückläufig verordneten Arzneimittelgruppen Insuline, Sulfonylharnstoffe (seit 2013 etwa um zwei Drittel zurückgegangen) und DPP-4-Hemmer. Glinide sind nur noch mit einer Substanz auf dem Markt vertreten. Die Metforminverordnungen stagnierten seit 2013 zunächst, sind aber in den letzten fünf Jahren wieder angestiegen. Zu den Antidiabetika mit stark steigenden Verordnungszahlen zählen die SGLT-2-Inhibitoren und GLP-1-Agonisten, die vermutlich aufgrund der Ergebnisse kardiovaskulärer Endpunktstudien und Empfehlungen in den Nationalen Versorgungsleitlinien 2022 jeweils um 40% mehr verordnet wurden.
Erneut haben die Nicht-Insuline einen deutlich höheren Kostenanteil als die Insulinpräparate. Dies liegt eindeutig an den teuren Präparaten der neueren Wirkstoffgruppen der SGLT2-Inhibitoren und der GLP-1-Agonisten [6].
Die Vielzahl an möglichen antidiabetischen Therapeutika erschwert die Auswahl der zweckmäßigen antidiabetischen Medikation für die Patienten. Im vorliegenden Leitfaden wird ausschließlich die wirtschaftliche Arzneimittelverordnung von Nicht-Insulinen beleuchtet.
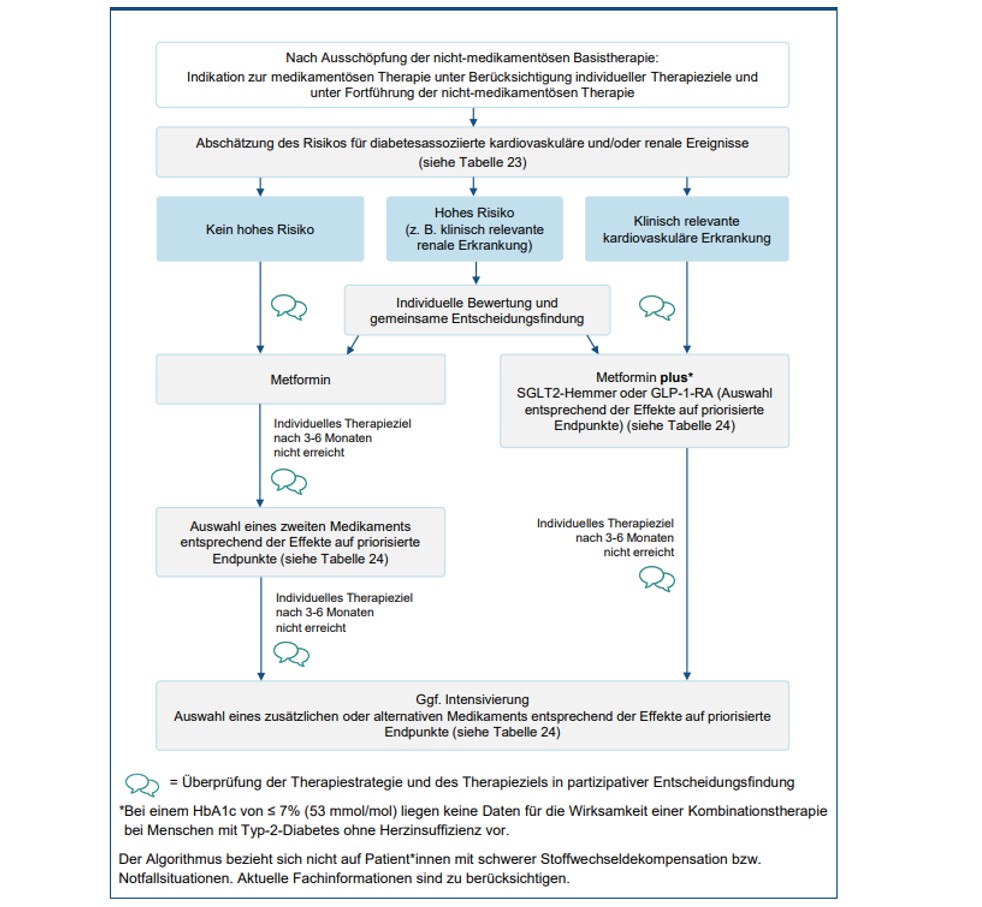
Grundsätzlich sollen vor jeder Therapie-Eskalation Ursachen für das Nichterreichen bisher vereinbarter Therapieziele evaluiert und berücksichtigt werden. Bevor die Therapie gemäß den Algorithmen eskaliert wird, ist es wichtig zu prüfen, ob es andere, behebbare Ursachen für das Nichterreichen von Therapiezielen gibt. Auch soll im Laufe der Erkrankung regelmäßig überprüft werden, ob die vereinbarte Therapie noch den aktuellen Therapiezielen entspricht oder angepasst werden muss. Dabei ist stets eine Abwägung zwischen potentiellem Nutzen und Schaden der Therapie nötig.
Abb. 1: NVL-Algorithmus zur medikamentösen Therapie des Typ-2-Diabetes [5]
3.3.1 Metformin
Die blutglukosesenkende Wirkung von Metformin, einem Biguanid-Derivat, beruht auf verschiedenen Mechanismen. Eine wichtige Rolle spielen unter anderem die Hemmung der hepatischen Glukoseproduktion (Glukoneogenese und Glykogenolyse), die verzögerte intestinale Glukoseresorption und Verbesserung der Insulinsensitivität in der Leber und peripheren Geweben. Die Empfehlungen, in denen Metformin als Erstwahlmittel bei Typ-2-Diabetes eingestuft wird, beruhen wesentlich auf den Ergebnissen der UKPD (United Kingdom Prospective Diabetes) 34-Studie [7]. Aufgrund der belegten Wirksamkeit hinsichtlich Stoffwechseleinstellung und makrovaskulärer Risikoreduktion sowie des geringen Einflusses auf Gewicht und Hypoglykämierate ist Metformin als First-line Antidiabetikum für die initiale Monotherapie des Typ-2-Diabetes zu bewerten [5].
Zu den Störwirkungen von Metformin gehören unter anderem Spontanberichte über Laktatazidose. Gefährdet scheinen insbesondere ältere Patienten zu sein, bei denen es aufgrund einer akuten Gastroenteritis zu einer Verschlechterung der Nierenfunktion kommt. Die Häufigkeit der Komplikation wird in Erhebungen mit bis zu 5,7 pro 10.000 Patientenjahre angegeben [8]. Metformin war in der Vergangenheit bereits ab einer mäßigen Niereninsuffizienz (Kreatininclearance unter 60 ml/min) kontraindiziert. Nach Abschluss eines europäischen Risikobewertungsverfahrens wurde im Herbst 2016 die Grenze für die Kreatininclearance, ab welcher Metformin kontraindiziert ist, jedoch auf GFR < 30 ml/min gesenkt. Patienten mit Nierenfunktionseinschränkung Grad 3b können seitdem auch mit Metformin behandelt werden, wenn die Dosis der Nierenfunktion entsprechend angepasst, die Nierenfunktion regelmäßig kontrolliert und Vorsichtsmaßnahmen beachtet werden. Bei akuter Nierenfunktionsverschlechterung unter Metformin sollte die Therapie pausiert werden [9].
Für die Monotherapie bei bestehender Metformin-Unverträglichkeit bzw. -kontraindikation sowie für die Kombinationstherapie bieten sich einige Alternativen an. Es ist jedoch im Hinblick auf eine wirtschaftliche Wirkstoffauswahl darauf hinzuweisen, dass eventuelle Unverträglichkeiten/Kontraindikationen gut dokumentiert werden müssen, da nicht jede Nebenwirkung (z.B. initiale gastrointestinale Beschwerden) als so schwerwiegend anzusehen ist, dass sie eine Therapie mit Metformin ausschließt.
Wenn Metformin allein nicht ausreicht, um das individuell festgelegte HbA1c-Ziel zu erreichen, sollte bei fehlenden kardiovaskulären Vorerkrankungen eine Kombination mit Sulfonylharnstoffen angeboten werden [10].
3.3.2 Sulfonylharnstoffe
Sulfonylharnstoffe (Glibenclamid, Gliclazid, Glimepirid) steigern die Sekretion von Insulin aus den B-Zellen der Pankreasinseln durch Blockade der Kalium-Kanäle. Eine noch vorhandene Funktionsfähigkeit des Inselorgans ist daher Voraussetzung für ihre Anwendung. Der HbA1c wird unter Sulfonylharnstoffen ähnlich stark gesenkt wie unter Metformin (um 1–2 Prozentpunkte), jedoch weisen sie insbesondere bei älteren Patienten den Nachteil der Hypoglykämie auf. In der DEGAM-Anwenderversion zur NVL werden sie als eine Option der zweiten oder dritten Stufe in Kombination mit Metformin genannt.
Es kann zu einem geringen Anstieg des Körpergewichts (um ca. 1,5 kg) kommen. Glibenclamid ist der bislang einzige insulinotrope Wirkstoff, für den ein positives Langzeitergebnis auf mikrovaskuläre diabetische Sekundärkomplikationen nachgewiesen wurde. Sulfonylharnstoffe können auch bei einer eingeschränkten Nierenfunktion eingesetzt werden, jedoch ist unterhalb einer Kreatinin-Clearance von 60 ml/min ihr Einsatz nur mit Vorsicht und in reduzierter Dosis angeraten.
Generell haben Sulfonylharnstoffe ein günstiges Kosten-Nutzenverhältnis und können durchaus eine wirtschaftliche Alternative darstellen. Bei Beachtung eines nicht zu niedrigen HbA1c-Zielbereichs sind sie unter Einhaltung der Vorsichtsmaßnahmen weiterhin eine vernünftige Wahl in der Therapie [11]. Sulfonylharnstoffe stellen im Rahmen der strafferen Blutzuckereinstellung bei jüngeren Patienten mit kürzerer Diabetesdauer und ohne wesentliche Begleiterkrankungen, wenn Metformin nicht eingenommen werden kann, nach wie vor eine Therapieoption dar. Die Kombination mit Metformin ist dann zu berücksichtigen, wenn Metformin allein nicht ausreicht und Insulin nicht akzeptiert wird [12].
3.3.3 SGLT2-Inhibitoren (Gliflozine)
SGLT2-Inhibitoren wie z.B. Empagliflozin oder Dapaglifozin hemmen spezifisch den Natrium-Glukose-Co-Transporter-2 (englisch Sodium-glucose co-transporter-2, SGLT2) im proximalen Tubulus der Niere, über den 90% der glomerulär filtrierten Glukose rückresorbiert werden, und erhöhen so die renale Glukoseausscheidung.
Auf Grund ihrer positiven Effekte auf kardiovaskuläre Endpunkte, Herzinsuffizienz, Niereninsuffizienz und Senkung der Mortalität nehmen sie eine bedeutende Rolle in der Behandlung der chronischen Herzinsuffizienz, chronischen Niereninsuffizienz sowie des Typ-2-Diabetes ein. Vor dem Einsatz dieser Medikamente bei Typ-2-Diabetes soll nach den aktuellen internationalen Leitlinien und der NVL in Deutschland eine Patienten-individuelle Risikoabschätzung hinsichtlich kardiovaskulärer und renaler Begleiterkrankungen vorgenommen werden.
Zwar wird in der aktuellen NVL von einer Stufen- oder Eskalationstherapie des Typ-2-Diabetes weitestgehend Abstand genommen, jedoch ist im Hinblick auf eine wirtschaftliche Verordnungsweise der initiale Einsatz eines SGLT-2-Hemmers nicht generell gerechtfertigt.
Zusätzlich zu Metformin kann ein SGLT-2-Inhibitor oder ein GLP-1-Agonist in Erwägung gezogen werden:
- wenn der individuelle HbA1c-Zielwert innerhalb von 3–6 Monaten nicht erreicht wird oder
- bei einem erhöhten Risiko für diabetesassoziierte und/oder renale Ereignisse oder
- bei Vorliegen einer klinisch relevanten kardiovaskulären Erkrankung.
Für viele Patienten ohne kardiovaskuläre Erkrankungen, die nach der bisherigen Datenlage keinen Vorteil von SGLT-2-Inhibitoren oder GLP-1-Agonisten haben, stellen nach wie vor Sulfonylharnstoffe eine Evidenz-gestützte Alternative dar [5].
Bezüglich der einzelnen Wirkstoffe der Gruppe der SGLT2-Inhibitoren und hier insbesondere der Indikation, der Evidenz, des Sicherheitsprofil und ggf. vorhandenen bundesweiten Praxisbesonderheiten wird auf den Leitfaden „SGLT-2-Hemmer (Gliflozine)- konsentierte Hinweise zur wirtschaftlichen Verordnung bei Erwachsenen“ verwiesen [13].
3.3.4 GLP-1-Rezeptoragonisten (GLP-1-RA)
Eine weitere Gruppe der Inkretinmimetika sind die Glucagon-like-Peptide-1-Agonisten (GLP-1-Agonisten). Sie haben eine ähnliche Aktivität wie das endogene Hormon, werden jedoch weniger schnell abgebaut. GLP-1-Rezeptoragonisten ahmen die Wirkung des körpereigenen Hormons GLP-1 nach, welches die glukoseabhängige Freisetzung von Insulin aus den ß-Zellen des Pankreas stimuliert und die Glukagon-Ausschüttung supprimiert. Darüber hinaus kommt es zu einer Verzögerung der Magenentleerung und Appetithemmung, was zur Gewichtsabnahme beiträgt. Erster zugelassener Vertreter der GLP-1-Agonisten war Exenatid (2007). Es folgten weitere Zulassungen für Liraglutid, Dulaglutid, Semaglutid und Tirzepatid.
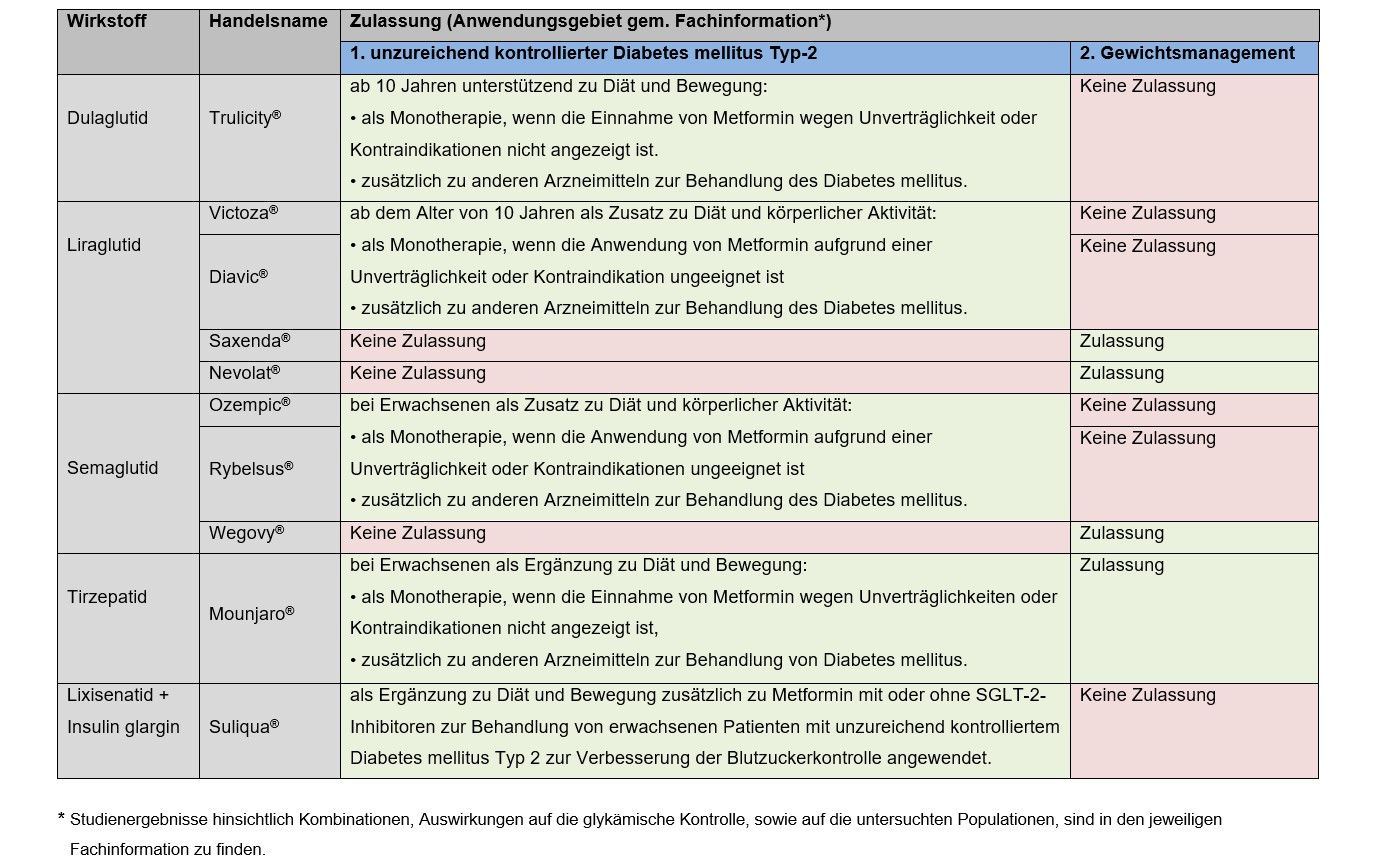
Beachten Sie bitte, dass die Wirkstoffe Liraglutid und Semaglutid unter verschiedenen Handelsnamen mit Zulassung in unterschiedlichen Indikationen in Verkehr sind: Victoza® (Liraglutid), Ozempic® (Semaglutid) und Rybelsus® (Semaglutid) sind für die Therapie des Typ-2-Diabetes zugelassen, Saxenda® (Liraglutid) und Wegovy® (Semaglutid) hingegen haben die Zulassung zur Gewichtsreduktion. Dulaglutid (Trulicity®) ist nur zur Therapie des Typ-2- Diabetes zugelassen. Tirzepatid wird unter dem Handelsnamen Mounjaro® vertrieben und ist sowohl zur Diabetestherapie als auch zur Gewichtsregulierung angezeigt. Lixisenatid (nur als Kombinationsarzneimittel mit Insulin glargin verfügbar, Handelsname Suliqua®) ist als Antidiabetikum in Kombination mit anderen Antidiabetika zugelassen.
Seit Mitte 2025 existiert ein erstes Liraglutid-Generikum zur Anwendung bei Typ-2-Diabetes (Diavic®). Ein weiteres Liraglutid-Generikum (Nevolat®), allerdings ausschließlich zur Gewichtsregulierung, ist seit Ende 2025 in Deutschland verfügbar. Beide Generika sind wie die Originale mit 6 mg/ml dosiert und als Fertigspritzen formuliert [14].
Tab. 2: Im Markt befindliche GLP-1-Agonisten mit der jeweiligen Zulassung
Die Anwendung der Präparate zur Gewichtsregulierung ist keine Kassenleistung und daher auch nicht Teil dieses Leitfadens.
Bezüglich des Sicherheitsprofils der GLP-1-Agonisten konnte in allen durchgeführten Studien eine höhere Rate an gastrointestinalen Nebenwirkungen beobachtet werden als unter Therapie mit Placebo. Zudem wird in den Fachinformationen von einem erhöhten Risiko für die Entwicklung akuter Pankreatitiden und Pankreaskarzinome berichtet. Es wird empfohlen, Patienten über die charakteristischen Symptome einer akuten Pankreatitis zu informieren. Sowohl FDA als auch EMA haben jedoch unabhängig voneinander die Befunde umfassend analysiert und stimmten darin überein, dass die gegenwärtige Datenlage keinen kausalen Zusammenhang zwischen der Anwendung von Inkretinmimetika und dem Auftreten von Pankreatitis bzw. Pankreaskarzinomen belegt [15].
Patienten mit Retinopathie sollten unter der Behandlung mit GLP-1-Agonisten auf die regelmäßigen augenärztlichen Kontrollen hingewiesen werden [5]. Nachdem Bedenken hinsichtlich eines möglichen erhöhten Risikos für die Entwicklung einer NAION (nicht arteriitische anteriore ischämische Optikus-Neuropathie) aufgekommen waren, hat der Pharmakovigilanz-Ausschuss (PRAC) der EMA untersucht, ob die Therapie mit Semaglutid-haltigen Präparaten wie Ozempic® mit einem erhöhten Risiko für diese Augenerkrankung verbunden ist. Die Überprüfung wurde mittlerweile abgeschlossen und der Verdacht bejaht. Die EMA hat daraufhin im Juni 2025 empfohlen, die Produktinformationen von Semaglutid-haltigen Arzneimitteln zu aktualisieren und NAION als eine Nebenwirkung mit der Häufigkeit »sehr selten« darin aufzunehmen. Wenn Patienten während der Behandlung mit Semaglutid einen plötzlichen Sehverlust oder eine rasche Verschlechterung des Sehvermögens bemerken, sollten sie sich unverzüglich an ihren Arzt wenden. Wenn eine NAION bestätigt wird, sollen sie die Behandlung mit Semaglutid abbrechen [16].
Neu ist zudem die Diskussion, ob die Anwendung von GLP-1-Agonisten zu einer Zunahme von suizidalen Gedanken oder gar Handlungen führen kann. Aufgrund eines Sicherheitssignals wurde dieser Zusammenhang von der Europäischen Arzneimittel-Agentur untersucht. Der Pharmakovigilanz-Ausschuss der EMA sieht jedoch keine Evidenz für einen kausalen Zusammenhang zwischen der Wirkstoffklasse der GLP-1-Rezeptoragonisten und suizidalen oder selbstverletzenden Gedanken und Handlungen [17].
Hinweis zum Off-label Einsatz bei Adipositas:
Es ist zu beachten, dass die Verordnung von GLP-1-Rezeptoragonisten, die ausschließlich für die Behandlung des Typ-2-Diabetes und nicht zur Gewichtsregulierung zugelassen sind, bei Patienten ohne Typ-2-Diabetes einen Off-Label-Use darstellt.
Selbst wenn es sich um eine zulassungskonforme Anwendung handelt, stellen Präparate zur Gewichtsregulierung keine GKV-Leistung dar und sind über die AM-RL Anlage II (Lifestyle AM) von der Verordnung ausgeschlossen. Der Verordnungsausschluss zu Lasten der gesetzlichen Krankenversicherung nach §34 SGB V gilt allerdings ausschließlich bei der Anwendung zur Gewichtsreduktion [18].
3.3.5 DPP-4-Inhibitoren (Gliptine)
Zu den Vertretern der Dipeptidyl-Peptidase-4-(DPP-4)-Inhibitoren gehören die in Deutschland zugelassenen Wirkstoffe Sitagliptin (2007, Januvia®), Vildagliptin (2008, Galvus®) und Saxagliptin (2009, Onglyza®). Gliptine sind sowohl als Mono- und teilweise auch als fixe Kombinationspräparate mit Metformin verfügbar [6]. Mittlerweile existieren Generika und z.T. liegen Rabattverträge nach §130a SGB V vor.
DPP-4-Inhibitoren wirken auf eine zellmembranständige Serinprotease, die den Abbau von Inkretinen einschließlich Glucagon-like Peptide-1 (GLP-1) regelt. Dadurch wird der Abbau von Inkretinhormonen, die nahrungsabhängig die Insulinsekretion stimulieren und die Glucagonfreisetzung hemmen, verzögert. Die zugelassenen Anwendungsgebiete gemäß Fachinformation beschränken sich auf Patienten, bei denen mit Diät und Bewegung keine ausreichende Blutzuckerkontrolle erzielt wurde. Außerdem wird grundsätzlich der vorrangige Einsatz von Metformin vorausgesetzt, es sei denn, es besteht eine Unverträglichkeit oder Kontraindikation für Metformin. Die Senkung des HbA1c liegt bei 0,5–0,8 Prozentpunkten [19] und ist damit geringer als bei der Erstlinientherapie mit Metformin [20]. Metformin, Sulfonylharnstoff oder eine Kombination dieser oralen Antidiabetika sind daher bei günstigen Kosten zu bevorzugende Therapiestrategien. Erst wenn eine Kombination von Metformin und einem Sulfonylharnstoff nicht zu einer angemessenen Blutzuckerkontrolle führt oder wegen Kontraindikationen bzw. Unverträglichkeiten nicht indiziert ist, kann die Kombinationstherapie mit einem Gliptin bei Patienten in Betracht kommen, die für eine Insulintherapie nicht geeignet sind oder bei denen eine Insulintherapie noch nicht angezeigt ist.
Bezüglich der Therapiesicherheit von Sitagliptin konnten in der TECOS-Studie Risikosignale für eine Verschlechterung der Nierenfunktion festgestellt werden [21]. So ist der Abfall der glomerulären Filtrationsrate im Verlauf der Studie ausgeprägter als unter Plazebo. Weiter konnte beobachtet werden, dass DPP-4 nicht nur Inkretine abbaut, sondern auch immunologisch wirksame Proteine. Unter Sitagliptin steigt daher die Gesamtrate infektiöser Erkrankungen (Atemwegsinfekte, Sinusitis, Harnwegsinfekte u.a.) um ein Drittel. Eine placebokontrollierte Studie mit Saxagliptin bei 16.492 Patienten mit kardiovaskulären Risikofaktoren zeigt eine erhöhte Inzidenz für Hospitalisierung wegen Herzinsuffizienz [22].
Zusammenfassend werden DPP-4-Inhibitoren gemäß aktueller NVL trotz fehlender Daten zu klinischen Endpunkten (wurden nicht untersucht), im Therapiealgorithmus als eine Option der zweiten oder dritten Stufe in Kombination mit Metformin genannt.
3.3.6 Glinide
Repaglinid ist der einzige zugelassene Vertreter der Glinidantidiabetika auf dem deutschen Markt. Es besitzt denselben Wirkmechanismus wie die Sulfonylharnstoffe und entspricht in Wirkung und Störwirkungen weitgehend den Sulfonylharnstoff-Antidiabetika. Die Blutglukose wird durch die Stimulation der Insulinsekretion an den pankreatischen Beta-Zellen gesenkt. Die Eliminationshalbwertszeit (1–2 h) von Repaglinid ist so kurz, dass es zu jeder Mahlzeit gegeben werden muss. Repaglinid wird hauptsächlich hepatisch eliminiert, was den Einsatz auch bei einer stärker eingeschränkten Nierenfunktion ermöglicht. Nach einer 2009 vom Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen (IQWiG) veröffentlichten systematischen Auswertung ist der Nutzen von Glinidantidiabetika wie Repaglinid bei Typ-2-Diabetes nicht belegt [23]. Seit 1. Juli 2016 ist Repaglinid durch einen Beschluss des G-BA nur noch eingeschränkt zu Lasten der Gesetzlichen Krankenversicherung (GKV) verordnungsfähig: Es darf nur noch bei niereninsuffizienten Patienten mit einer Kreatininclearance <25 ml/min verordnet werden, für die andere orale Antidiabetika nicht infrage kommen und eine Insulintherapie nicht angezeigt ist.
In der aktuellen NVL spielt Repaglinid im Therapiealgorithmus keine Rolle. Auch in der verbleibenden Verordnungsnische eines Typ-2-Diabetes mit schwerer Niereninsuffizienz kann Repaglinid allenfalls als Reservemittel zur Symptomvermeidung bei sehr hohen Glukosewerten, angesehen werden, wenn Insulin nicht akzeptiert wird [24].
3.3.7 Thiazolidindione (Glitazone)
Analog der Glinide sind Glitazone seltenen Sondersituationen vorbehalten und wurden im Rahmen der Leitlinienerstellung nicht näher betrachtet. Pioglitazon wurde ohne publizierte nachprüfbare Nutzenbelege in den Handel gebracht. Es handelt sich um ein umstrittenes Therapieprinzip, von dem seit Sommer 2011 auch die deutsche Arzneimittelbehörde abrät. Seitdem darf Pioglitazon nur noch in begründeten Einzelfällen zu Lasten der GKV verordnet werden. Das BfArM empfiehlt, Pioglitazon wegen einer Risikoerhöhung für Blasenkarzinome nicht mehr zu verschreiben [25].
Rosiglitazon wurde bereits 2010 vom Markt genommen, da es in Studien das Risiko für Myokardinfarkte signifikant erhöhte.
3.4 Allgemeine Hinweise zur wirtschaftlichen Arzneimittelverordnung bei Typ-2-Diabetes
- Nach wie vor ist eine Lebensstiländerung mit Ernährungsanpassungen, körperlicher Aktivität und soweit möglich einer Gewichtsreduktion die Grundlage der Diabetestherapie. Diese nichtmedikamentösen Maßnahmen gelten als Basistherapie auf jeder Therapiestufe und werden auch bei geriatrischen Patienten empfohlen. Bei der Ersteinstellung übergewichtiger Menschen mit Typ-2-Diabetes bzw. Prädiabetes ist eine relevante Absenkung des HbA1c-Wertes häufig allein durch eine Veränderung der Ernährung und einer Steigerung der körperlichen Aktivität möglich. Erst wenn diese Maßnahmen den Blutzucker nicht ausreichend kontrollieren, ist eine Arzneitherapie des Typ-2-Diabetes erforderlich.
- Der Zielbereich für eine medikamentöse Senkung des HbA1c wird von den Fachgesellschaften unterschiedlich gesehen. Die DEGAM empfiehlt eine medikamentöse Senkung der Blutglukose bei Patienten ohne kardiovaskuläre Erkrankungen erst ab einem HbA1c >7,5 % [10]. Der HbA1c-Wert hat im höheren Lebensalter einen geringeren Stellenwert bei Therapieentscheidungen. Die Einstellung des HbA1c sollte sich an der jeweiligen Patientengruppe orientieren und in einem Zielkorridor von HbA1c 6,5% bis <8,5% liegen.
- Zwar wird in der aktuellen NVL von einer Stufen- oder Eskalationstherapie des Typ-2-Diabetes weitestgehend Abstand genommen, jedoch ist im Hinblick auf eine wirtschaftliche Verordnungsweise der initiale Einsatz eines SGLT-2-Hemmers oder eines GLP-1-RA nicht generell gerechtfertigt.
- Bei fehlenden Kontraindikationen und Ausschöpfung aller nichtmedikamentösen Maßnahmen wird in den Leitlinienempfehlungen zur Behandlung des Typ-2-Diabetes mellitus einheitlich Metformin als Medikament der ersten Wahl angesehen. Aufgrund der belegten Wirksamkeit hinsichtlich Stoffwechseleinstellung und makrovaskulärer Risikoreduktion sowie des geringen Einflusses auf Gewicht und Hypoglykämierate ist es als First-line Antidiabetikum für die initiale Monotherapie des Typ-2-Diabetes zu bewerten [5].
- Für die Monotherapie bei bestehender Metformin-Unverträglichkeit bzw. -kontraindikation sowie für die Kombinationstherapie bieten sich einige Alternativen an. Wenn Metformin allein nicht ausreicht, um das individuell festgelegte HbA1c-Ziel zu erreichen, sollte bei fehlenden kardiovaskulären Vorerkrankungen eine Kombination mit Sulfonylharnstoffen angeboten werden [10]. Wird der individuelle HbA1c-Zielwert innerhalb von 3–6 Monaten nicht erreicht oder bei einem erhöhten Risiko für diabetesassoziierte und/oder renale Ereignisse oder einer klinisch relevanten kardiovaskulären Erkrankung, können zusätzlich zu Metformin ein SGLT-2-Inhibitor oder GLP-1 Analogon in Erwägung gezogen werden. Für viele Patienten ohne kardiovaskuläre Erkrankungen, die nach der bisherigen Datenlage keinen Vorteil von SGLT-2-Inhibitoren oder GLP-1-Agonisten haben, stellen nach wie vor Sulfonylharnstoffe eine Evidenz-gestützte Alternative dar [5].
- Die Zulassungen der GLP-1-Agonisten beschränken sich auf Patienten mit unzureichend kontrolliertem Typ-2-Diabetes. Von einem unzureichend kontrollierten Diabetes ist auszugehen, wenn das patientenindividuelle Therapieziel für HbA1c über einen Zeitraum von 3-6 Monaten nicht erreicht wird. Der Zielbereich für den HbA1c- Wert liegt zwischen 6,5 % und 8,5 %.
Der Einsatz als Monotherapie ist lediglich in den Fällen vorgesehen, wenn Metformin kontraindiziert oder wegen anhaltender Unverträglichkeiten ungeeignet ist. In allen anderen Fällen sieht die Zulassung eine Kombinationstherapie mit anderen blutzuckersenkenden Arzneimitteln, einschließlich Insulin, vor.
Ein initialer Einsatz nach Ausschöpfung der nicht-medikamentösen Basistherapie ist im Therapiealgorithmus der NVL nach individueller Bewertung nur bei einem hohen Risiko für diabetesassoziierte und kardiovaskuläre und/oder renale Ereignisse in Kombination mit Metformin vorgesehen.
Bei einem HbA1c von ≤ 7% (53 mmol/mol) liegen keine Daten für die Wirksamkeit einer Kombinationstherapie bei Menschen mit Typ-2-Diabetes ohne Herzinsuffizienz vor. Zu beachten sind hier jedoch immer die individuellen Therapieziele. - Empagliflozin als bundesweite Praxisbesonderheit ist im Rahmen der statistischen Prüfung bei entsprechendem Einsatz ab dem ersten Behandlungsfall als Praxisbesonderheit anzuerkennen.
- Zur wirtschaftlichen Verordnung der weiteren SGLT-2-Hemmer sei auf den Therapieleitfaden „SGLT-2-Hemmer (Gliflozine)- konsentierte Hinweise zur wirtschaftlichen Verordnung bei Erwachsenen“ verwiesen. [13]
- Beachten Sie den vorrangigen Einsatz von verfügbaren Generika sowie bestehende Rabattverträge.